
導(dǎo)讀
雄激素剝奪治療(ADT)是前列腺癌最重要的基礎(chǔ)治療之一,其主要目標是將血清睪酮降低并穩(wěn)定維持于去勢水平以下。前列腺癌的睪酮管理是指通過規(guī)律的睪酮檢測和結(jié)果分析,指導(dǎo)前列腺癌臨床診療策略的選擇,是前列腺癌診療工作的重要組成部分。
近年來的前列腺癌相關(guān)研究不斷為睪酮管理帶來理念更新,內(nèi)容涉及睪酮去勢水平的定義、不同檢測方法的對比,以及合理的監(jiān)測頻率等。
20世紀90年代,多將“<50ng/d”作為睪酮的去勢標準。2013年,一項研究結(jié)果首次證實將睪酮控制到更低水平(≤32ng/dl),可顯著延緩去勢抵抗性前列腺癌出現(xiàn)時間。基于相關(guān)研究,2014~2020版歐洲泌尿外科學會(EAU)前列腺癌指南均提出“控制睪酮水平穩(wěn)定<20ng/dl可作為判斷去勢水平的更合適數(shù)值。2018版《加拿大復(fù)發(fā)和轉(zhuǎn)移性前列腺癌睪酮抑制治療共識》也將“<20ng/dl”作為新的去勢標準。
睪酮的代謝及影響因素
成人睪酮的生理功能包括維持肌容量和肌力、骨骼密度和強度,以及維持正常的性欲及性功能等。
血液中睪酮大多以結(jié)合形式存在,僅1%~3%以游離形式存在,兩種形式之間存在動態(tài)平衡游離睪酮是發(fā)揮生物活性的主要物質(zhì),血清睪酮進入前列腺后,可直接或經(jīng)5α還原酶作用轉(zhuǎn)化為雙氫睪酮活化雄激素受體,繼而發(fā)揮調(diào)節(jié)前列腺生長與功能的作用。
影響睪酮水平的常見因素包括:1隨著年齡增長,血清總睪酮緩慢下降,但FT下降更為顯著,一般認為其最高水平在20~29歲,40歲以后顯著下降,70~80時達最低水平;過度肥胖促進局部糖皮質(zhì)激素轉(zhuǎn)化,破壞HPGA功能,導(dǎo)致睪酮水平下降;應(yīng)激、快波睡眠時間延長可導(dǎo)致睪酮升高;鋅元素缺乏降低睪酮水平。
睪酮管理的臨床推薦
1. 強調(diào)睪酮管理需貫穿前列腺癌患者的診斷、評估、治療及療效評價全程,是疾病管理的重要組成部分,并向患者及家屬普及睪酮管理的意義,取得配合。
2. 在重要的疾病階段起始點(確診、復(fù)發(fā)、新發(fā)轉(zhuǎn)移、CRPC)和治療切換點(治愈性治療、ADT方法改變、化療等其他治療起始)需檢測睪酮作為基線值,為后續(xù)診療提供參考。
3. 前列腺癌ADT期間和確診CRPC時,仍以睪酮水平<50ng/dl(1.735nmol/L)為去勢標準;但ADT期間深度降酮即將睪酮水平抑制到<20ng/dl(0.694nmol/L)的更低水平,可作為臨床更佳治療預(yù)后和調(diào)整治療的參考指標。
4. 推薦ADT開始前及治療8個月內(nèi)每月規(guī)律檢測睪酮;使用LHRHa類藥物的初期,應(yīng)使用雄激素受體拮抗劑以避免藥理性睪酮“閃爍”引起的潛在疾病進展風險;隨著病情進入平穩(wěn)狀態(tài),可延長睪酮檢測間隔至每3~6個月1次;次/或?qū)⒉G酮檢測與PSA檢測同步進行。
5. 發(fā)現(xiàn)睪酮逃逸時可換用其他抑制睪酮生成藥物或轉(zhuǎn)為手術(shù)去勢。
6. 確診CRPC后,仍需維持睪酮在去勢水平。
7. 臨床初始應(yīng)用新型長效ADT制劑或新型內(nèi)分泌治療藥物時,應(yīng)注意保證睪酮檢測頻率,以確保睪酮控制效果及降低失訪率。
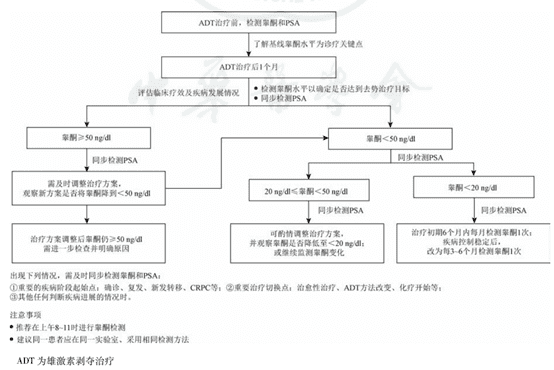
ADT治療期間的睪酮監(jiān)測和管理規(guī)范化流程圖
結(jié)語和展望
睪酮管理是前列腺癌全程管理的重要組成部分。睪酮達去勢水平后,降低睪酮至更低水平(<20ng/dl)可作為判斷前列腺癌患者更佳預(yù)后和調(diào)整治療的參考標準,未來需開展更多前瞻性研究進一步探討其應(yīng)用期間的睪酮規(guī)范管理和更低睪酮水平的遠期臨床獲益。
近年來,多種新型內(nèi)分泌藥物相繼進入國內(nèi)市場,并在前列腺癌患者的疾病更早階段與傳統(tǒng)ADT疊加應(yīng)用,這將為睪酮的管理帶來更多新問題。理論上,以阿比特龍為代表的雄激素合成抑制劑可降低血清睪酮;恩扎盧胺、阿帕他胺等藥物屬非甾類雄激素受體拮抗劑可通過負反饋調(diào)節(jié)升高睪酮。鑒于新型內(nèi)分泌藥物在中國臨床應(yīng)用時間較短,其應(yīng)用期間的睪酮規(guī)范管理策略仍有待進一步探討和補充。
標簽:百科







